BACKGROUND
La GSK-3β è un enzima fondamentale per molteplici funzioni cellulari: si stima che più di 100 proteine siano bersaglio di tale chinasi, non altro che una macchina molecolare che opera attaccando un gruppo chimico (fosfato) ad altre molecole modificandone la funzione. Una anomala attivazione di tale enzima può determinare, pertanto, malfunzionamento delle proteine target e promuovere l’insorgenza di varie patologie. Nel caso delle malattie neurodegenerative, come la malattia di Alzheimer, o di quelle neuropsichiatriche come il disturbo bipolare, si osserva una iperattivazione dell’enzima GSK-3β, che a cascata coinvolge proteine chiave, quali ad esempio la proteina tau, ed una aberrante attivazione della via “Wnt/β-catenina”, coinvolta nell’ingresso di vari virus, come quello dell’Herpes Simplex 1 e Sars-CoV-2. Controllare l’attivazione di questo enzima in specifiche aree cerebrali potrebbe, quindi, contrastare l’insorgenza di tali malattie.
Il litio è un potente inibitore della GSK-3β e rappresenta, ad oggi, il farmaco di elezione nel trattamento di patologie neuropsichiatriche quali il Disturbo Bipolare. Le concentrazioni di litio necessarie per contrastare i meccanismi molecolari responsabili delle malattie neurodegenerative o le infezioni virali che interessano il sistema nervoso centrale sono più elevate di quelle considerate accettabili in termini di rapporto rischio/beneficio, limitando in maniera importante le applicazioni terapeutiche di tale catione.
«La nostra sfida - spiega il professor Piacentini - è stata quella di sviluppare un dispositivo che permettesse di sfruttare le potenzialità terapeutiche del litio senza determinarne effetti avversi e che potesse essere veicolato in maniera sito-specifica evitando la somministrazione sistemica».
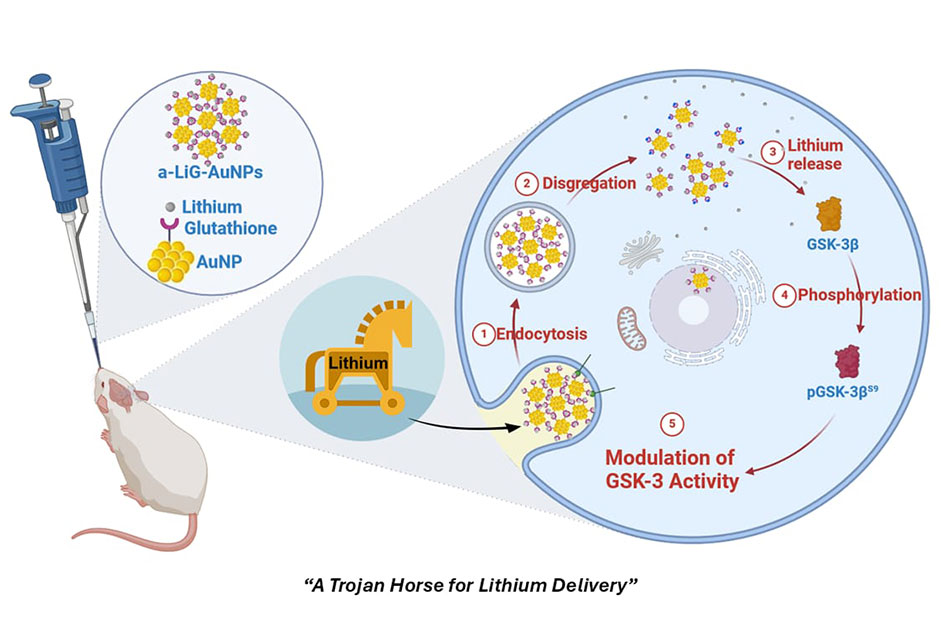
«Le nanoparticelle d’oro - aggiunge il professor Buonerba - rappresentano il tool ottimale per questo tipo di strategia. Esse possono essere funzionalizzate con glutatione che, da un lato favorisce la formazione di aggregati che entrano facilmente nelle cellule e, dall’altro, permette di legare molecole o ioni, come il litio. Una volta che gli aggregati di nanoparticelle entrano nelle cellule, questi vengono disgregati e il litio viene scaricato dentro le cellule, consentendo di ottenere concentrazioni terapeutiche efficaci di tale ione a fronte di basse dosi di somministrazione».
«Inoltre - continua il professor Piacentini - la via intranasale rappresenta un percorso elettivo per raggiungere direttamente il cervello senza passare per il circolo sistemico, ottimizzando quindi la sicurezza del nostro nanodispositivo. L’oro, metallo inerte e già dimostrato essere innocuo nei sistemi biologici, viene eliminato mediante escrezione renale limitando il suo accumulo nel cervello a seguito di somministrazioni ripetute nel tempo».
«La versatilità di questo nuovo vettore farmaceutico è straordinaria - evidenzia il professor Antonio Buonerba. Le nanoparticelle sviluppate possono essere caricate con diversi principi attivi farmacologici e sono in grado di sfuggire alle difese cellulari biologiche, permettendo il trasporto mirato di questi verso gli specifici siti attivi fisiologici».
«In questo lavoro - spiega la dottoressa Giulia Puliatti, primo autore dello studio insieme al professor Buonerba - abbiamo dimostrato che 5 giorni di somministrazione di nanoparticelle d’oro funzionalizzate con glutatione e rivestite di litio (chiamate LiG-AuNPs) sono in grado di inibire significativamente l’attività della chinasi GSK-3β nell’ippocampo dei topi e lo stesso trattamento ripetuto per 2 mesi comporta una significativa regressione del deficit di memoria esibito da un modello murino di malattia di Alzheimer, analizzato a livello comportamentale e molecolare».
VERSO NUOVE POSSIBILITÀ DI CURA
«Ad oggi i farmaci a base di litio sono ampiamente utilizzati per il trattamento delle malattie neuropsichiatriche - sottolinea il professor Claudio Grassi - ma purtroppo non sono esenti da importanti effetti collaterali. Assunto per via orale sotto forma di compresse, il litio raggiunge il cervello attraverso la circolazione sanguigna e, pertanto, finisce per esercitare effetti tossici su altri organi quali, ad esempio, il rene e la tiroide. Riuscire ad ottenere concentrazioni efficaci di litio nelle cellule nervose, mediante una somministrazione ‘mirata al cervello’ di basse dosi dello ione grazie all’ausilio delle nanoparticelle d’oro, rappresenta quindi un’innovazione importante per la messa a punto di nuove e più sicure modalità di trattamento dei pazienti. Riteniamo che il nostro tool nanotecnologico possa consentire lo sviluppo di nuovi approcci terapeutici non solo per le patologie di interesse psichiatrico ma anche per quelle malattie neurodegenerative e virali nelle quali un’alterata attività della GSK-3β a livello cerebrale gioca un ruolo chiave».
«Infine - conclude il professor Alfonso Grassi - la facilità di sintesi delle nostre nanoparticelle semplifica il processo produttivo, mantenendo bassi i costi di realizzazione di un prodotto da immettere, nel futuro prossimo, sul mercato farmaceutico».